‐文献名-
Parks AL, Frankel DS, Kim DH, Koh D, Kramer DB, Lidstone M, Fang MC, Shah SJ.
Management of atrial fibrillation in older adults. BMJ. 2024;386(e076246):1-12.
doi:10.1136/bmj-2023-076246
‐要約-
長いのでポイントを列挙
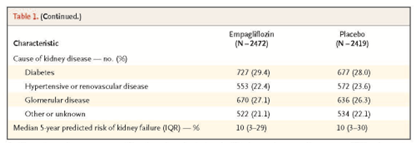
1.心房細動患者の80%は65歳以上で、加齢に伴い指数関数的に増え、65歳の人の1/3はいつか心房細動は細動を発症する(図1 ここでは省略)。
2.高齢の心房細動患者の39〜51%がフレイル。多疾患併存やポリファーマシーもよくある。
3.高齢者への心房細動のケアは個別化するアプローチが必要(図2)
4.高齢者にはガイドラインをそのまま適用できないことも多い
5.多疾患併存のある患者の治療負担や望まないケアを減らす効果的な方法として、 Patient Priorities Careがある。
6.予後が短い場合や、治療の害が利益を上回ると思われる場合には、治療の縮小も必要。
7.脳梗塞やTIAの既往のない一般住民への心房細動のスクリーニングの効果は不明(図3省略 図4)。
8.ライフスタイルへの介入がフレイルや多疾患併存のある高齢心房細動患者に有用かどうかは不明。予後が短い患者にはしないほうがよさそう。(図5)
9.高齢者の心房細動の症状は、若年者と異なり、疲労感や倦怠感が主症状になることもある。
10.ACC/AHA/ACCP/HRSによる2023年のガイドラインでは、レートコントロールよりもリズムコントロールの方が推奨されている。フレイルや多疾患併存のある人への一般化はまだ考えなくてはならないが、高齢者も比較的研究されている。
11.リズムコントロールの方法として、カテーテルアブレーションの方が抗不整脈薬よりも良く、元気な高齢者には推奨できる。フレイルや多疾患併存がある場合には個別に検討。(図6)
12.HFrEFが併存する場合は、早期のリズムコントロールによる洞調律の維持が推奨される。抗不整脈薬よりもカテーテルアブレーションの方が良い。
13.75歳以上のすべての心房細動患者は脳梗塞リスクが高いと考えられ、抗凝固療法が推奨されるが、高齢者、フレイルでポリファーマシーの患者、認知機能障害がある人などへの抗凝固療法についてのエビデンスは十分ではない(図7省略)。
14.出血リスク予測スコア(HAS-BLED、HEMORR2HAGES、ATRIAなど)は使用しないことを推奨。
15.抗凝固療法にはワーファリンよりもDOACを推奨。アスピリンは避けるべき。
16.重度のCKD、出血リスクが高まる薬剤の併用、低体重、重度の出血の既往がある高齢者への、低用量エドキサバンは有用そう。
17.eGFR30-59mL/minまたはstage3aや3bのCKDがある患者への抗凝固療法は有益だが、末期腎不全患者への抗凝固療法の有益性を示した研究はない。
18.抗凝固療法に関連する出血リスクを減らす方法として、抗血小板薬の併用を中止すること、高血圧やNSAIDsなどの出血リスク因子を減らす、複数の抗血栓薬を使うときはPPIを併用することがある(図8 省略)。
19.心房細動に関連する脳梗塞を予防するために高齢者に抗凝固療法を導入したり維持したりするには、注意深く個別化した意思決定が必要(図9)。
20.左心耳閉鎖は、元気な高齢者にはガイドラインに則って推奨、フレイルや多疾患併存の患者は個別に検討、終末期患者には適応なし。
21.アップルウォッチでのスクリーニング、第Ⅺa因子や第Ⅻa因子を標的にした抗凝固療法、カテーテルアブレーション後の抗凝固療法、適切なshared decision makingの方法について、現在も研究中。
<Introduction>
心房細動は高齢者に多いですが、ほとんどのRCTやガイドライン、レビューは他と切り離した単独の心房細動に焦点を当てています。心房細動だけに罹患している高齢者には適しますが、心房細動患者の多くはフレイルで、少なくとも1つの老年症候群や、複数の疾患を持ち、治療の優先順位も変わります。こうした高齢患者に、既存のエビデンスやガイドラインを、コンテクストを無視してそのまま当てはめることは、利益より害が上回るかもしれず、患者にとって最も問題になるものを扱っていないかもしれません。このレビューは、心房細動と多疾患併存の高齢者のマネジメントにおける主要な進歩を扱い、目的を指向するアプローチを使います。まず、心房細動患者が持つ併存疾患や老年症候群を特徴づけます。続いて心房細動のケアの領域のエビデンスを調査しました。
<Method>
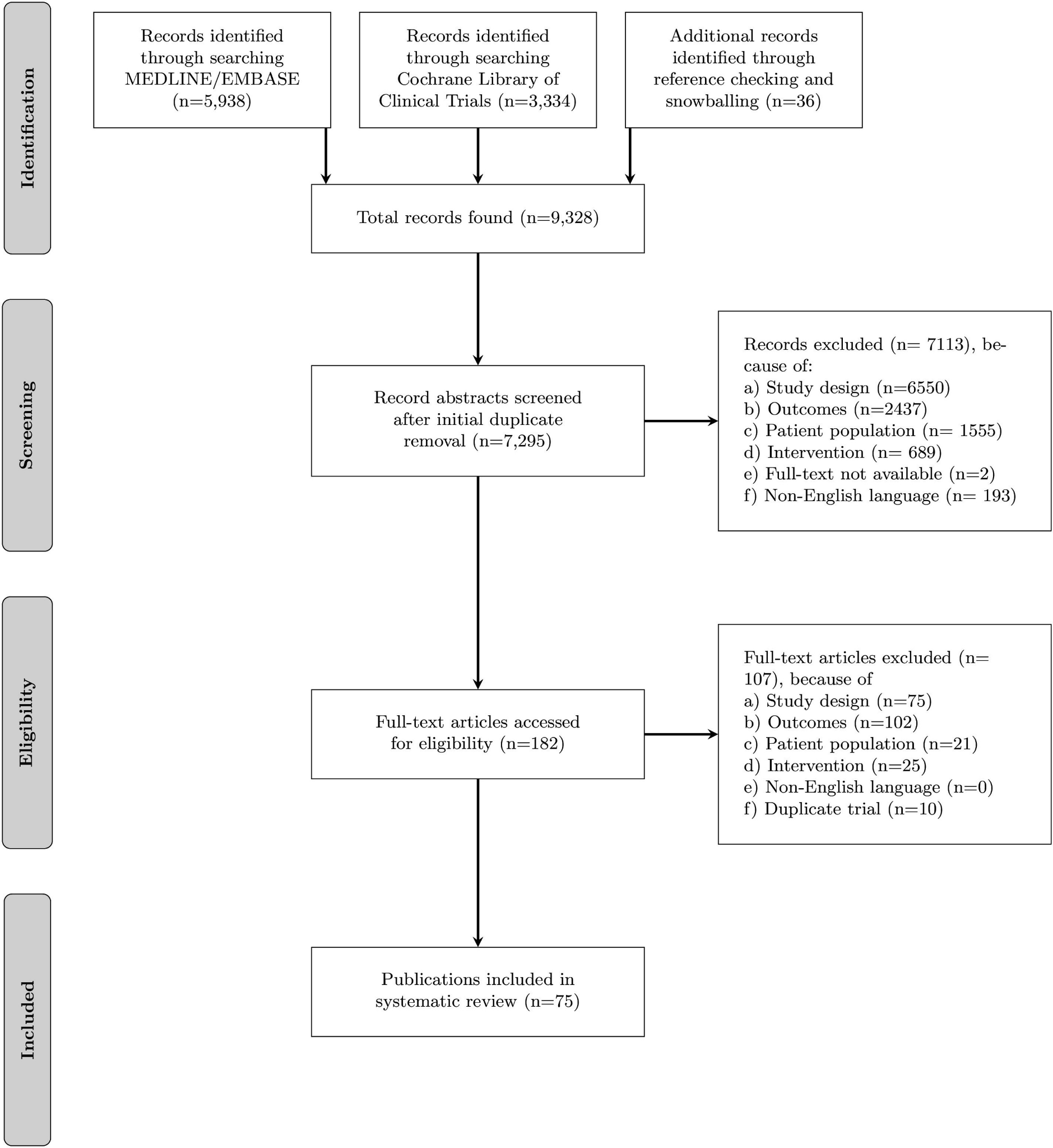
私達は、特に高齢者に関連する入手可能な心房細動の文献を包括的に含むように文献調査をしましたが、現存するすべての文献は調べませんでしたし、効果を見積もるためのメタアナリシスもしませんでした。このレビューはPRISMA(Preferred Reporting Items for Systematic Reviews and Meta-Analyses)2020ガイドラインに沿って作成しました。医学司書が、Ovid MEDLINE(1946年から現在まで)、Embase.com(1947年から現在まで)、Web of Science Core Collection(1900年から現在まで)、Cochrane Central Register of Controlled Trials(CENTRAL) via Ovid(1991年から現在まで)、ClinicalTrials.gov(1999年から現在まで)を使って、2023年5月に文献検索しました。検索方策には、高齢者、RCTs、心房細動の統制語彙およびフリーテキストの同義語を組み込みました。言語による制限はしませんでした。2010年以降の文献に絞り込み、方法や年齢でのフィルターを使用しました。同定された研究はすべて EndNoteとEPPI-Reviewerを使用して重複を排除して組み合わせ、Covidence systematic review softwareにアップロードしました。少なくとも2人の研究者が抄録を調査し、それぞれの章の著者が全文を読んで関連性を調べました。2024年8月にESCのガイドラインが改定されており、私達も2021年のESCガイドラインに代わって新しいものを参照しました。
<高齢者における心房細動と多疾患併存の疫学>
心房細動は加齢と関連していて、心房細動患者の80%は65歳以上です。心房細動が高齢者に多いというだけでなく、様々な危険因子で調整した後でも、心房細動の発症率は年齢とともに指数関数的に増えています。Framingham Studyの分析では、65歳の人の心房細動の生涯有病率は33%でした。
他の高齢者に集中する多くの疾患同様に、心房細動も老年症候群と併存しています。たとえば、心房細動をもつ高齢アメリカ人のコホートでは、20%が転倒で外傷を受傷し、25%がなんらかのADLで介助が必要でした。フレイルは高齢の心房細動患者によくあります(39〜51%)。心房細動をもつ高齢患者は、多疾患併存やポリファーマシーの強い負担も負っています。
病気の累積的な負担は、心房細動を新規に診断された高齢者の診断後1年以内の死亡率が20〜25%になるとの複数の疫学研究に示されています。これらを踏まえると、心房細動をもつ高齢者のケアには、複数の慢性疾患をもつ高齢者の、疾患のすべての負担や個々の健康目標を考慮した、全人的アプローチが必要です。
<高齢者の心房細動マネジメントの個別化>
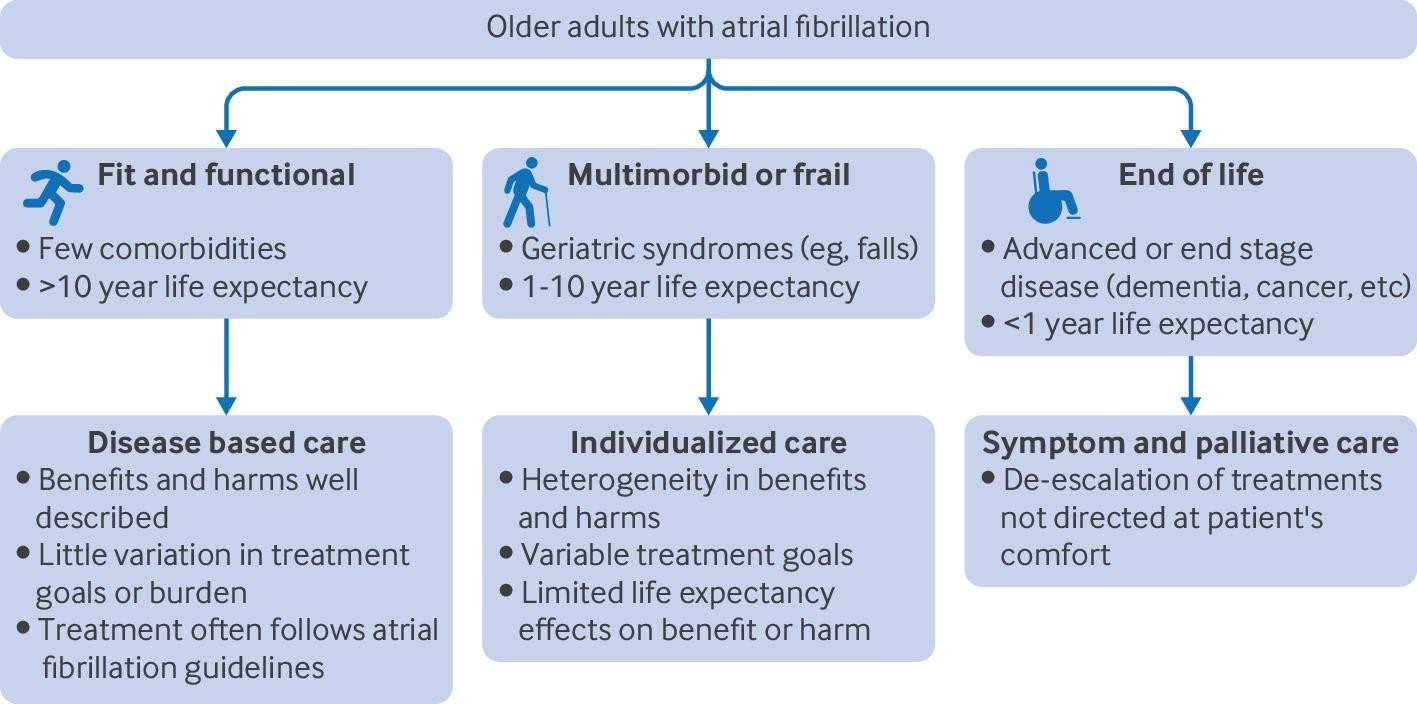
高齢者での心房細動の増加やケアの複雑さは多くの人に馴染みのあるものとなっていますが、臨床ケアを最適に適応させる方法は依然として課題です。最新の心房細動ガイドラインはこれらの複雑さを認めていて、統合された多職種からなる医療機関、「個別化されたケアのパッケージ」、患者の価値観を探ること、shared deci- sion makingを推奨しています。しかしこれを実装するのかは難しいままです。図2に心房細動の高齢患者のマネジメントを、多疾患併存、フレイル、予後によって個別化するアプローチの提案を示します。
Fig 2 | Proposed approach to tailor clinical management of atrial fibrillation (AF) to older adults
<ガイドラインを高齢者に外挿することの問題点>
心房細動ガイドラインは心房細動の症状を減らしたり、合併症を予防したりすることを目的とする臨床試験から得られたエビデンスに基づいて推奨が作られています。一般に疾患のガイドラインは、同じ健康目標を共有する単一の疾患をもつ患者に適しています。
多疾患併存やフレイルのある高齢者がRCTには組み込まれていないので、高齢者全員にガイドラインの推奨を単純に外挿することは困難です。高齢者を含んだ研究でも、雑多な健康状態を捉えきれていないでしょう。高齢者の多疾患併存や関連する治療負担は、生活機能やQOLにマイナスの影響をおよぼし、心房細動の治療薬や手術によって害が生じる危険性もあります。多疾患併存やフレイルのある高齢者は、健康上の優先課題が競合することが多く、健康目標にも大きな個人差があります。
<個別化されたケアを実践するアプローチ>
心房細動での全人的な個別化されたケアを実践するエビデンスに基づいた方法の1つに、患者の健康問題の優先事項を考慮して治療を組み立てることがあります。適切な意思決定をするために、臨床家はそれぞれの患者の機能やフレイルの状態を把握するべきです。身体機能やフレイルさを評価する方法には、Clinical Fraility ScaleやComprehensive geriatric assessmentがあります。予後を推定することは難しいですが、 ePrognosisは多疾患併存のある高齢者の予後を推定するためのツールとして使えます。こうした情報で、個別の特定の目標による最適の治療計画は決められます。こうしたアプローチの一例として、Patient Priorities Careがあります。これは今までのところ、多疾患併存のある患者の治療負担や望まないケアを減らす最も効果的な方法です。
<治療の縮小>
死期が近い高齢者では、症状やQOLや快適さに焦点を当てた緩和ケアが適切です。治療関連の害の方が利益よりも上回ると考えられるときや、病気が進行して治療の利益がよくわからなくなった時には、治療の縮小を検討すると良いです。抗凝固薬の中止は、患者の予後や出血リスクと塞栓リスク、QOLに影響する要素、患者や家族の意向を考慮して個別に考えるべきです。
<住民レベルの計画的なスクリーニング>
脳梗塞やTIAを起こした患者に心房細動のスクリーニングをする有用性は明らかですが、一般住民に対するスクリーニングのエビデンスはわかっていません。スクリーニングによって心房細動の診断率が上がることはRCTで示されていますが、それによって脳梗塞が減少したり健康状態がより良くなったりするかどうかは、まだわかりません。
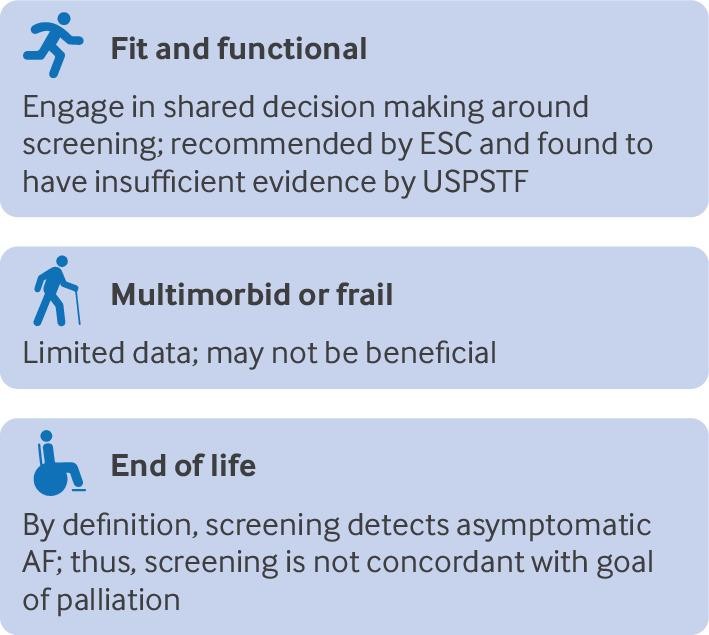
Fig 4 | Summary of recommendations for atrial fibrillation screening in older adults. ESC=European Society of Cardiology; USPSTF=United States Preventive Services Task Force
<2次予防のためのライフスタイルへの介入>
元気な患者の心房細動を予防したり治療したりするために、肥満の予防、体重を減らすこと、中等度の運動、血圧のコントロール、そしてもしかしたら禁酒も有用であることがわかっています。これらの知見を多疾患併存やフレイルのある高齢者にどのように適用するかは、さらなる研究が必要です。余命が短い人にとって、生活習慣を変えることは目的にかないそうもありませんし、得られる利益も限られたものになりそうです。
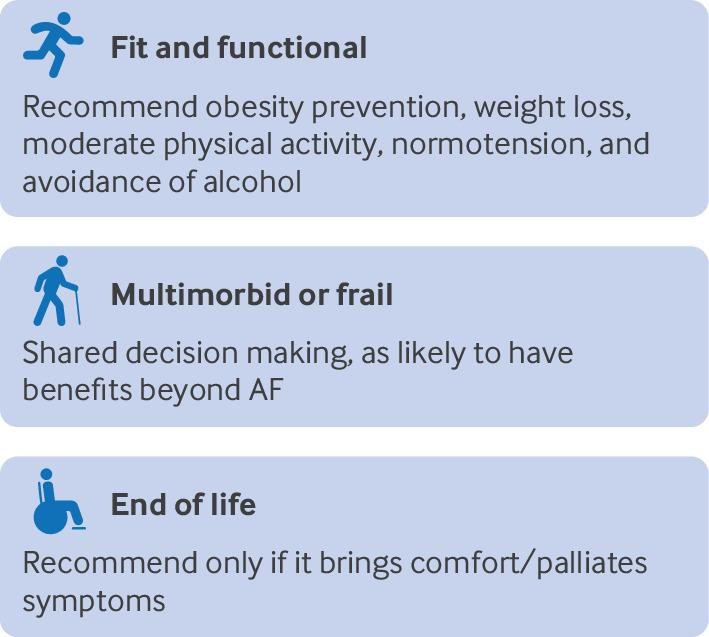
Fig 5 | Summary of recommendations for atrial fibrillation (AF) lifestyle interventions
<心房細動の症状と臨床的特徴>
心房細動の症状は非特異的で間欠的なものかもしれないし、高齢者は若年者と異なって出現するかもしれません。動機、めまい感、息切れ、胸部不快感はすべての年齢で見られますが、高齢者では疲労感や全身倦怠感を主な症状として自覚しやすいです。失神は他の伝導疾患が合併していなければ稀です。多疾患併存がある高齢者では、こうした症状の原因を心房細動に求めることが、より難しくなります。
症状を緩和することは多くの心房細動患者にとって主要な目標です。様々な治療戦略がQOLに与える影響について、医師や患者が報告したものが、多くの臨床研究で使われてきましたし、患者が有効であると報告した方法は臨床的にも使われています。患者が報告する心房細動に特有のアウトカムを長期にわたって臨床実践に統合したところ、点数が悪いほど心房細動の負担や医療利用の頻度が高く、レートコントロールよりもリズムコントロールを使用することが多いことに相関していました。患者の経験を体系的に測定することで、心房細動の症状とQOLへの幅広い影響を把握し、治療目標を明確にし、推奨される治療法を導き出し、進歩し続けることに役立ちます。
心房細動やその治療による症状がある患者は、専門医に紹介することが有益な可能性があります。
<レートコントロールとリズムコントロール>
ACC/AHA/ACCP/HRSによる2023年の心房細動の診断と治療のガイドラインは、発作性および持続性心房細動の両方に対して、以前のガイドラインと比較して、リズムコントロールの方をレートコントロールよりも多く、そしてより早く使用する方向に大きく動き出すことを推奨しました。これらのガイドラインに影響を与えている研究では、リズムコントロールは幅広い臨床指標を改善し、安全性も確認されています。フレイルや多疾患併存のある人への一般化はまだ考えなくてはなりませんが、高齢者も比較的研究されています。
これらのガイドラインは高齢者のリズムコントロールを、心不全がある場合は強い推奨、症状があったり診断後1年以内であったりする場合には中等度の推奨としています。ガイドラインは現代の技術を活用した厳格な臨床試験を引用していて、それらの試験は一貫してレートコントロールよりもリズムコントロールの方を臨床結果が良いため支持しています。例えば、レートコントロールに比べて、リズムコントロールの方が、心血管死や脳卒中、心不全増悪による入院や急性冠症候群が顕著に少なかったため(3.9vs5.0/100人年;ハザード比0.79,95%CI0.66~0.94)、平均5年の追跡期間で試験が中途終了となったものもあります(EAST-AFNET4)。ただし、QOLは両群間で差がありませんでした。
EAST-AFNET4はリズムコントロールに抗不整脈薬とカテーテルアブレーションの両方を含みましたが、他の研究では、カテーテルアブレーションの方が洞調律を維持でき、治療合併症頻度が少ないという点で優れていることがわかりました。例えばCABANA試験です。
早期のデータでは、カテーテルアブレーションが心房細動のある高齢者の認知機能を改善するかもしれないということが示唆されました。観察研究では心房細動と脳容量の減少や認知機能の低下、認知症発症リスクの上昇に関連していることが示されていました。洞調律に回復するとこれらのリスクを減らすことができるのかどうかは、活発に調べられる分野になっています。96人の抗不整脈薬を使用している心房細動患者を、薬剤継続とアブレーションに無作為に割り付けた研究では、アブレーション群は治療後に14%で認知機能が低下していましたが、これは主に麻酔や無症候性の脳塞栓によるもので、1年以内に回復しており、さらに、1年後には14%に認知機能の改善が見られました。一方薬剤群では1年後の認知機能の改善は見られませんでした。
これらの研究の平均年齢は、70歳だったり68歳だったりするので、65歳以上の元気な心房細動患者には早期のリズムコントロール、とくにカテーテルアブレーションを提案するのが良いでしょう。しかし、カテーテルアブレーションにするか抗不整脈薬にするかは、多疾患併存やフレイルな高齢者には個別に考えるべきです。抗不整脈薬は他の薬剤と広範囲な相互作用がありますし、肝障害や腎障害のある場合には薬剤代謝が変動します。これらの危険性は、特に多疾患併存やフレイルな患者では、短期的な麻酔やアブレーション治療合併症と注意深く比較する必要がありますし、個別の状況に応じた治療を検討する必要があります。併存疾患が多かったり、予後が短いと想定されたりする患者では、早期リズムコントロールによって、寿命やQOLへの利益はあまりないと考えるかもしれませんが、必ずしもそうではありません(例えば心不全などについては)。多疾患併存によって心房細動のある高齢者でのリズムコントロールは難しくなりますが、心房細動による負担を減らすことは大きな影響をもつものかもしれません。人生の最終段階では、リズムコントロールが症状緩和以外の重要性をもつとは、あまり考えられません。
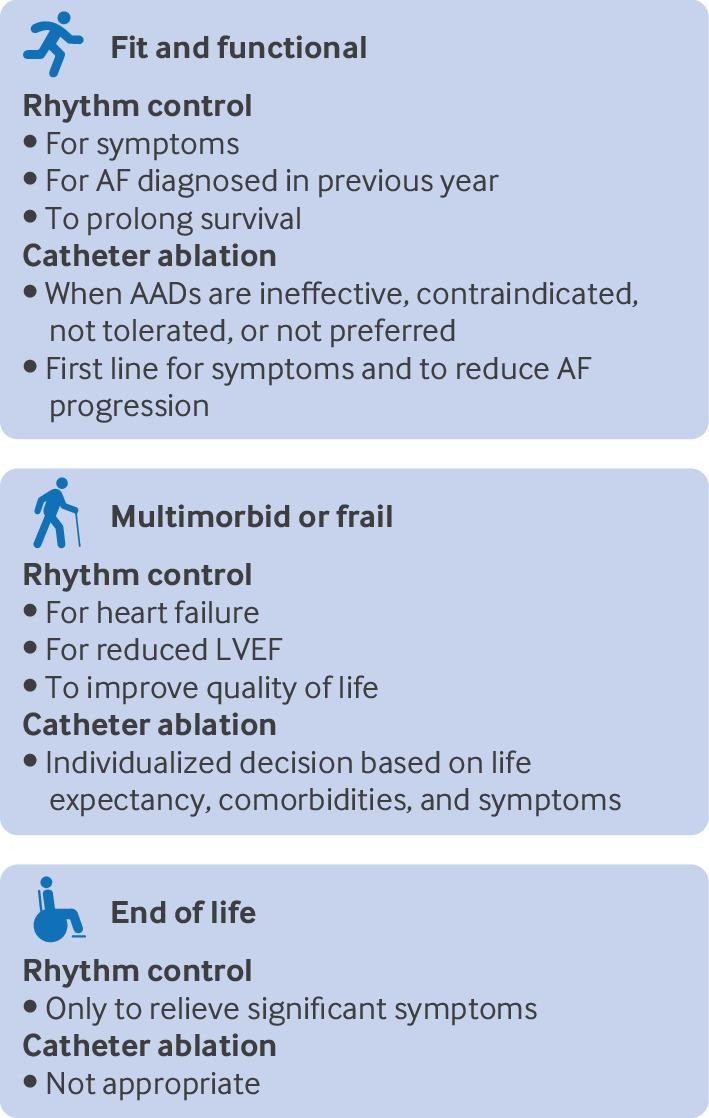
Fig 6 | Summary of recommendations for rate and rhythm control in older adults with atrial fibrillation (AF). AAD=anti-arrhythmic drug; LVEF=left ventricular ejection fraction
<心不全と心房細動>
心不全のある患者の心房細動の治療は特別な考慮を必要とします。というのは、心不全と心房細動は相互に影響しあい、心不全があると心房細動の頻度は増え、心房細動は心不全の予後を悪化させるからです。心房細動と心不全が併存することは多いです。この状況での推奨される治療は、主に若い世代のデータから外挿されたものです。HFrEFが併存する場合は、早期のリズムコントロールによる洞調律の維持が推奨され、しかも、長期の抗不整脈薬の使用よりはカテーテルアブレーションの方を検討すべきです。HFrEFでは非ジヒドロピリジンCa拮抗薬(ジルチアゼムやベラパミル)や、ドロネダロンは、医原性の悪影響があるので禁忌です。フレカイニドやソタロールは、催不整脈作用によって禁忌です。ポリファーマシーや副作用症状を減らすもう一つの方法は、ペースメーカーの挿入を行い、房室接合部のアブレーションを検討するものです。
<塞栓予防のための経口抗凝固剤の利害のバランスをとること>
経口抗凝固薬は心房細動に関連する脳梗塞を減らしますが、出血が増えるという代償もあります。加齢は利害評価、もしくは「真の臨床的利益」の多くの面に影響します。加齢とともに脳梗塞のリスクは高まりますが、抗凝固による出血リスクも高まります。心房細動が多い層であるのに、塞栓予防の抗凝固療法のRCTは80歳以上の人をあまり入れていません。さらに、人が年をとって平均寿命に達するにつれて、抗凝固療法による脳卒中の予防の潜在的利益は、それと拮抗する脳梗塞以外に関連する死亡や障害の危険によって減ってしまいます。最近のコンセンサスガイドラインでは、75歳以上のすべての患者を、心房細動関連脳梗塞の高リスク群で抗凝固療法が推奨されるとしています。しかし最近出されたESCガイドラインでは、「高齢者、フレイルでポリファーマシーの患者、認知機能障害がある人などへの抗凝固療法についてのエビデンスは十分ではない」と明白に述べています。2023年のACC/AHA/ACCP/HRSガイドラインで、出血する人としない人を識別できないことや、可逆的な出血の危険因子を軽く見積もることなどを理由に、出血リスク予測スコア(HAS-BLED、HEMORR2HAGES、ATRIAなど)を使用しないことを推奨していることは重要です。ガイドラインは一般に、ワーファリンよりもDOACを推奨しています。効果が同等で、全般的に出血率が低く、薬物相互作用が少なく、モニタリングの必要性が少ないからです。妥協案として抗凝固薬の代わりにアスピリンを使おうとするのは避けるべきです。出血リスクは同等なのに脳梗塞予防効果は劣っており、心房細動にアスピリンを使用するのはClassⅢの危険であると考えられているからです。2023年に更新されたアメリカ老年医学会のBeers Criteriaでは、抗凝固療法を始めるならワーファリンよりもDOAC、さらにその中でもアピキサバンが出血リスクが低いので推奨されています。抗凝固薬同士の比較はまだ進行中です。
すべての高齢者に抗凝固療法は真の利益があるというパラダイムに異を唱えた研究もあります。平均寿命を超えた人には、抗凝固療法の利益は、拮抗する心房細動以外の原因による死の危険のために大幅に減っていくことを示した研究もあります。これらの研究から、最近のガイドラインを適用するには、加齢や多疾患併存の負担を考慮にいれるもっと微妙なアプローチが必要と言えます。
<フレイルや多疾患併存の高齢者での抗凝固療法>
最近の研究から、多疾患併存やフレイルの高齢者での抗凝固療法についてのガイダンスが得られています。重度のCKD、出血リスクが高まる薬剤の併用、低体重、重度の出血の既往がある日本人高齢者への、低用量エドキサバンの研究(ELDERCARE-AF)では、低用量エドキサバンは出血リスクや全死因死亡を増やさず、脳卒中や全身の塞栓症を減らすことがわかりました。メディケアのデータを調査した結果、あらゆるフレイルのグループで、アピキサバンはワーファリンと比べて、死亡、脳梗塞、大出血を1/3減らすことがわかりました。ダビガトランやリバロキサバンはフレイルではない患者にのみ、イベント発生率を減らしました。出血リスクの少なさからはアピキサバンが推奨されていますが、Beersクライテリアではワーファリンを使用している患者には、DOACに切り替えないことを推奨しています。ワーファリンからDOACに切り替えたら、出血合併症が増加し、塞栓合併症の減少が見られなかったとするFRAIL-AF研究によるものです。
<慢性腎臓病>
eGFR30-59mL/minまたはstage3aや3bのCKDがある患者への抗凝固療法は有益な可能性があります。末期腎臓病の心房細動患者に対して抗凝固療法が本当に有益だと示したRCTはありません。透析療法中の患者に抗凝固薬を使うと、出血率や死亡率が高くなります。末期腎臓病患者への抗凝固療法とプラセボを比較する試験がいくつか行われている最中です。末期腎臓病に対しては、DOACはワーファリンに代わる許容可能な選択肢であると示した研究はありますが、DOACが良いのかワーファリンが良いのかはまだ不明です。ガイドラインでは、軽度から中等度のCKD患者にはワーファリンやDOACの使用を支持し、重度のCKD患者にはワーファリンまたはアピキサバンの使用を弱く推奨しています。
<抗凝固療法に関連する出血>
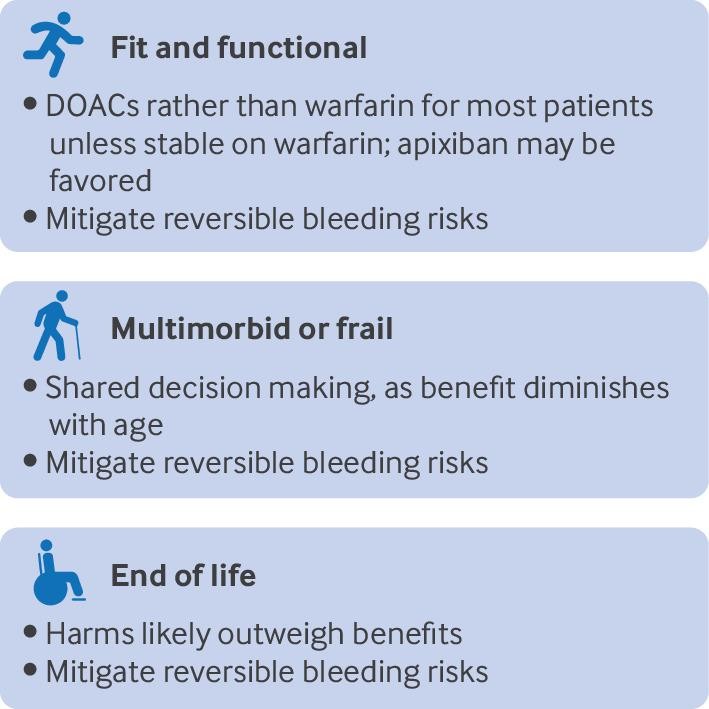
抗凝固療法に関連する出血リスクを減らす方法がいくつかあります。ひとつは抗血小板薬の併用を中止することです。抗血小板薬を併用しても塞栓リスクは減りませんが、出血リスクは1.5―2倍に上がるのです。専門家のコンセンサスガイダンスでは、心血管疾患予防のためのアスピリンを避けること、高リスクの状況のごく短期間(最近PCIしたばかりなど)を除いて3剤療法(DAPT+抗凝固)を避けること、抗血小板薬と抗凝固薬の適応となる患者(虚血性心疾患でACSやPCI後6−12ヶ月経過しているなど)への抗凝固薬単剤療法とすること、頸動脈ステントを留置していない脳血管疾患の患者に抗凝固療法単剤とすることを推奨しています。他の方法として、高血圧やNSAIDsなどの可逆的な出血危険因子は減らし、複数の抗血栓薬を使用する場合には消化管出血を予防するためにPPIを検討します。
結局、心房細動に関連する脳梗塞を予防するために高齢者に抗凝固療法を導入したり維持したりするには、注意深くて個別化した意思決定が必要となります。余命が長い患者には抗凝固療法は最大限の効果があり、その利益は年とともに減っていきます。フレイルや多疾患併存を含めて多くの患者にはワーファリンよりはDOACの方が好まれますが、意思決定には値段や患者の好みや服用回数なども考慮して意思決定をしなくてはなりません。終末期の患者、つまり抗凝固療法の利益が見込めないくらい余命が短かそうな患者や害に苦しみそうな患者は、抗凝固薬をやめるよう努力すべきです。
<左心耳閉鎖>
左心耳閉鎖の合理性は、心房細動患者の左房内血栓のほとんどが左心耳にできるという観察研究に由来します。左心耳閉鎖にはワーファリンと同等の脳塞栓予防効果があり、出血合併症を避けられます。左心耳閉鎖とDOACの比較にはしっかりしたデータがなく、さらなる研究結果に注意することが求められます。
左心耳閉鎖の効果と安全性は、ワーファリンと比較した非劣性試験が2つ行われています。当初はこれら2つの結果は相反するものでした。PROTECT AF試験では、脳梗塞、全身の血栓症、心血管死に非劣性が示されましたが、それより高齢で、もっと多疾患併存の患者を組み込んだPREVAIL試験では、非劣性は示せませんでした。これらの相違はその後5年間の患者レベルでのメタアナリシスで弱められ、プライマリアウトカムで2.8/100人年(左心耳閉鎖)vs3.4/100人年(ワーファリン)でした。さらに、左心耳閉鎖群に割り付けられた患者は、脳出血や脳卒中後遺症が少なかったのです。
左心耳閉鎖がワーファリンと比較して研究されたことは重要です。アピキサバンなどもっと脳梗塞予防に効果的で出血リスクも低いものが好まれるようになって、ワーファリンの使用頻度は減っています。DOACと比較しても左心耳閉鎖の有効性は非劣性であるとするエビデンスも前に出されましたし、いまもRCTが進行中です。
あらゆる処置と同じように、合併症は高齢者で特に考えなくてはいけないことです。PREVAIL試験では4.2%の合併症発生率でした。左心耳閉鎖装置の認可後の観察分析では、この割合は2.2%まで下がっています。80歳より高齢の患者では、入院中の有害事象がもう少し高くなっていました。入院中の転機を超えて、フレイルな高齢者には、顕著に高い有害事象が退院後に生じていました。
左心耳閉鎖から最も利益を得られそうな患者を選ぶことに関しては、実践とエビデンスに大きな溝があります。経口抗凝固療法なしと比べると、左心耳閉鎖がもっとも確実に塞栓リスクを減らしそうですが、出血リスクを考慮して経口抗凝固療法を受けそうもない患者は、認可前の研究からもっとも除外されていそうです。老年症候群が併存している患者は、経口抗凝固療法を受けることが少なそうですが、重大な処置合併症が起きる頻度が増しそうですし、左心耳閉鎖後に永続するアスピリンでの抗血小板療法による出血合併症の頻度も増しそうです。
メディケアやメディケイドは、長期の経口抗凝固療法が禁忌の患者にのみ、左心耳閉鎖を認めています。2023年のACC/AHA/ACCP/HRSガイドラインでも、左心耳閉鎖は、不可逆的な原因によって長期の抗凝固療法が禁忌の患者に中等度推奨、出血リスクが高い患者に弱い推奨となっています。
高齢患者も左心耳閉鎖を支持するRCTに多く組み込まれました。だから元気な患者は、65歳以上であってもガイドラインの推奨に従って左心耳閉鎖を提案されるべきです。多疾患併存やフレイルな高齢患者は、リスクへの耐性や、処置合併症、長期的な抗凝固療法以外の抗血栓療法の利益を考慮して、個別に意思決定するとよいでしょう。終末期の患者は、左心耳閉鎖の適応にはなりません。
<新しい治療法>
新しい治療戦略は、高齢の心房細動患者のケアに影響するかもしれません。スクリーニングでは、消費者のデバイスによって心房細動の発見を強化して治療することが脳梗塞を減らすかどうかという基本的な疑問が、アップルウォッチでのスクリーニングに無作為割付するHEARTLINE研究が行われています。出血リスクを減らしつつ血栓リスクを減らすと仮定される、これまでと異なる凝固カスケード蛋白(第Ⅺa因子、第Ⅻa因子)を標的にした新規抗凝固薬について行われているRCTでは、高齢の心房細動患者が主要な被験者層になっています。カテーテルアブレーション後の最適な抗凝固療法については、抗凝固療法が中止可能なのかどうかも含めて調べられています。また、持続的なリズムモニタリングに並行して間欠的に抗凝固療法を行う方法も調べられています。最後に、Shared decision makingは高齢者に対しては賞賛される目標ですし、ガイドラインで推奨もされますが、最適なフォーマットや、それが臨床結果を改善するかどうかについてはいくつかの研究が行われています。
<ガイドライン>
心房細動のマネジメントについてはいくつかの臨床ガイドがあります。このレビューを編集している最中、2024年8月にRSCガイドラインが更新されました。これらのガイドラインは、認知機能障害のある心房細動の高齢患者の抗凝固療法についての性を設けていて、今回報告したエビデンスやガイダンスに概ね一致しています。2024年のESCガイドラインでは、フレイルや認知症を含む多疾患併存のある高齢患者について、抗凝固療法を支持するエビデンスが欠如していることを新たに強調しています。2023年のACC/AHA/ACCP/HRSガイドラインでは、Shared decision makingについての短い議論を組み込みましたが、主にそれが臨床的な良い結果につながるというデータが欠けていることに焦点が当てられていました。2021年に更新された英国からのNIHのガイダンスでは、心理的サポート、社会的サポート、つながりを作る情報、教育的な情報を含む、「個人化されたケアのパッケージ」を求めています。最後に、2020年のCanadian Cardioligy Societyのガイダンスは、心房細動ケアの多職種モデルも提案しています。
‐結論-
心房細動を何十年も研究して臨床現場でケアしてきたので、罹患率や死亡率は劇的に減ってきました。ですが、心房細動は加齢に伴う典型的な疾患のままですし、疾患に焦点を当てたアプローチだけを使うと、木を見て森を見ないことにつながってしまいます。私達は現存するエビデンスを雑多なニーズをもつ高齢者に適用する枠組みを提示しました。そうする中で、増え続ける心房細動の高齢患者に対して個別化されたケアを行うためのエビデンスを強化することに努力する必要性にも焦点を当てました。複雑でフレイルな患者を組み込み、高齢者にとって認知のような重要な結果を調べる、実践的な研究が増えているので、励まされます。今後の臨床研究では、厳格な除外基準を設けず、私達の現場で出会う患者を反映した患者を組み込んで行うべきです。患者の主観的結果を使う事が増えており、臨床研究のプライマリアウトカムやセカンダリアウトカムも、狭い臨床的イベントから抜け出して患者の優先項目に基づくべきです。エビデンスに基づくshared decision makingは、抗凝固療法についてもっとも進んでいますが、心房細動のマネジメントのあらゆる面に広げるべきです。ほとんどの心房細動患者は、他にも複数の悩ましい慢性疾患のガイドラインに従わなくてはならないことを認識して、私達は患者の目標を思考したケアに基づいた枠組みを受け入れなくてはなりません。
【開催日】2025年9月3日